武汉偏光成像纺锤体起偏器
近年来,随着玻璃化冷冻技术的不断发展,成熟卵母细胞纺锤体的冷冻保存研究取得了进展。研究表明,采用玻璃化冷冻法冷冻保存的成熟卵母细胞,在解冻后其纺锤体和染色体的形态及功能均能得到较好的保持。这主要得益于玻璃化冷冻过程中避免了冰晶形成对细胞的损伤,以及冷冻保护剂对细胞的有效保护。然而,值得注意的是,尽管玻璃化冷冻法在提高解冻存活率和妊娠成功率方面取得了成效,但仍存在一些问题。例如,冷冻过程中纺锤体的微管结构可能受到低温的影响而发生解聚,导致染色体分离异常。此外,冷冻保护剂的毒性也可能对卵母细胞造成一定的损伤。为了克服这些问题,研究者们进行了大量的实验和优化工作。例如,通过改进冷冻保护剂的配方和浓度,降低其对细胞的毒性;通过优化冷冻速率和程序,减少冷冻过程中对细胞的机械损伤;以及通过筛选和评估不同冷冻载体和保存时间对卵母细胞冷冻效果的影响,寻找好的冷冻保存条件。纺锤体在细胞分裂过程中展现出惊人的自我组装能力。武汉偏光成像纺锤体起偏器
在生殖医学领域,卵母细胞的冷冻保存技术一直是研究的热点之一。尤其是针对卵母细胞内部高度复杂且精细的纺锤体结构,其冷冻过程中的稳定性与完整性直接关系到解冻后卵母细胞的存活率及发育潜能。纺锤体作为卵母细胞内部的关键结构,由微管等高分子物质有序排列而成,具有双折射性。这种特性使得纺锤体在偏振光下能够呈现出独特的形态和特征,从而被Polscope等偏振光显微镜捕捉并观察。双折射性纺锤体的形态、稳定性和完整性对于卵母细胞的正常减数分裂及胚胎发育至关重要。上海纺锤体实时成像纺锤体兼容大部分显微镜纺锤体形成缺陷是多种遗传疾病的共同特征。
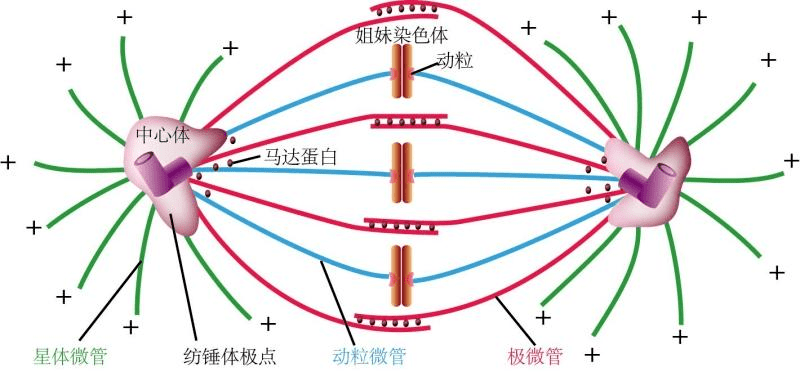
染色体
当细胞从间期进入有丝分裂期,间期细胞微管网络解聚为游离的αβ-微管蛋白二聚体,再重组成纺锤体,介导染色体的运动;分裂末期纺锤体微管解聚,又重组形成细胞质微管网络。
可分为:动粒微管:连接染色体动粒于两极的微管。
极间微管:从两极发出,在纺锤体中部赤道区相互交错的微管。
星体微管:中心体周围呈辐射分布的微管。
染色体的运动依赖纺锤体微管的组装和去组装。在这一过程中动粒微管与动粒之间的滑动主要是依靠结合在动粒部位的驱动蛋白和动力蛋白沿微管的运动来完成。极微管在纺锤体中部交错,有些分布在极微管之间特殊的双极马达蛋白,其中2个马达蛋白沿一条微管运动,另2个马达结构域沿另一条微管运动。由于2条微管分别来自二极,故极性相反。当双极驱动蛋白四聚体沿微管向正极运动时,纺锤体二极间距离延长。反之纺锤体距离缩短。
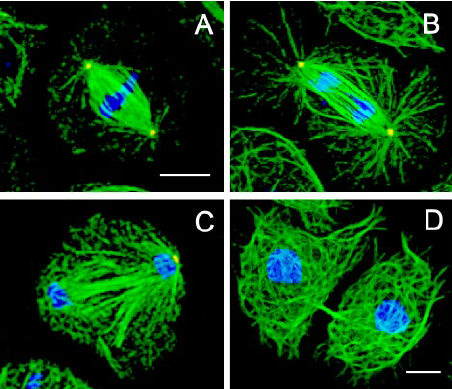
纺锤体是卵母细胞在减数分裂过程中形成的一种微管结构,负责精确分离染色体。然而,纺锤体对环境温度、渗透压等外部条件极为敏感,在冷冻保存过程中容易发生损伤,导致染色体分离异常,进而影响卵母细胞的发育潜力和受精后的胚胎质量。因此,如何有效监测和评估冷冻过程中纺锤体的变化,成为纺锤体卵冷冻研究的重要课题。纺锤体实时成像技术的出现,为这一问题的解决提供了可能。纺锤体实时成像技术主要利用高分辨率显微镜结合荧光标记技术,对卵母细胞内的纺锤体进行实时、动态的观察和记录。常用的荧光标记方法包括使用绿色荧光蛋白(GFP)标记微管蛋白,以及利用特定抗体对纺锤体相关蛋白进行染色。通过这些方法,研究者可以清晰地观察到纺锤体的形态、位置、动态变化等信息,从而准确评估冷冻过程中纺锤体的稳定性和完整性。纺锤体微管与染色体之间的相互作用是细胞分裂的重点事件。
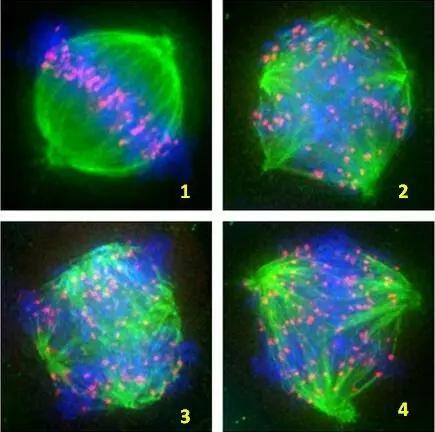
卵母细胞的冷冻保存技术一直是研究的热点之一,特别是针对不同成熟阶段的卵母细胞,如MI期卵母细胞的冷冻保存。MI期卵母细胞具有独特的生物学特性和发育潜能,其纺锤体的稳定性和形态对于后续的受精和胚胎发育至关重要。因此,针对MI期纺锤体卵冷冻的研究不仅具有理论价值,更具有重要的临床应用前景。MI期卵母细胞的纺锤体由微管组成,这些微管结构精细且脆弱,容易受到冷冻过程中温度变化和渗透压变化的影响而发生损伤。纺锤体的损伤不仅会影响卵母细胞的正常发育,还可能导致受精失败或胚胎发育异常。纺锤体在细胞分裂中的功能受到细胞内外环境的共同影响。北京非侵入式成像纺锤体揭示卵母细胞关键结构
纺锤体形成的精确性对于维持生物体遗传稳定性至关重要。武汉偏光成像纺锤体起偏器
近年来,研究者们通过不断优化冷冻保护剂的配方和浓度,发现某些特定成分的组合能够减轻冷冻过程中纺锤体的损伤。例如,紫杉醇等细胞骨架保护剂在稳定纺锤体微管结构方面表现出色,成为冷冻保存中的重要辅助手段。Polscope偏振光显微成像系统的应用,使得对双折射性纺锤体的动态观察成为可能。通过实时监测冷冻过程中纺锤体的形态变化,研究者能够更准确地评估冷冻效果,并优化冷冻保存条件。此外,偏光成像技术还能够提供纺锤体异常率的量化数据,为临床应用提供可靠依据。武汉偏光成像纺锤体起偏器
上一篇: 美国辅助生殖纺锤体透明带
下一篇: 昆明哺乳动物纺锤体透明带