江西环状DNA平台
总的来说,eccDNA的形成是依赖于DNA的序列特征、复制过程和DNA损伤的修复的。从目前已有的研究进展来看,就序列特征而言,串联重复序列会更容易造成eccDNA的形成;并且大部分的eccDNA有段重复序列,但是也有相当的部分没有重复序列,不能与任何附近的序列发生重组;高GC、转录刺激区域,像R-loop形成和修复促进eccDNA的形成;同源重组会切除重复DNA产生序列更大的eccDNA。而就DNA损伤修复而言,研究发现致ai物会提高eccDNA的水平,同时一些特异的DNA损伤修复蛋白是eccDNA形成所必需的,但是还有一些是非必需的。测序后首先可以得到一个详尽的环状DNA注释表格。江西环状DNA平台
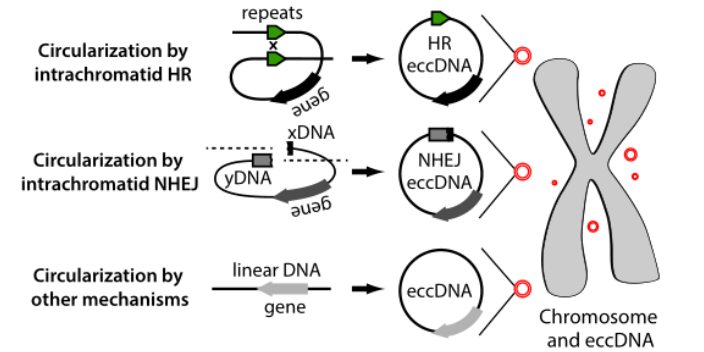
案例1:孕妇血浆中胎儿环状DNA 的特征是:呈甲基化状态以及被清chu 近期,NIPT之父卢煜明教授团队开发了一种环状DNA 甲基化分析的测序方案,通过对不同产后时间点的胎儿环状DNA含量的评估,研究了胎儿环状DNA的体外清chu效率。作者还发现血浆中的胎儿 环状DNA 与母体 环状DNA 相比甲基化程度相对较低。此外,和胎儿线性DNA类似,胎儿环状DNA在分娩后从母血中迅速清chu。总之,该团队基于转座酶和m5C位点酶学转化方法开发出了环状DNA甲基化测序技术,并揭示了孕妇血浆中的胎儿环状DNA甲基化状况,为环状DNA的深入研究及新型分子标志物的开发提供了新的技术手段。中国台湾环状DNA平台研究发现eccDNA环化多来源于ai基因。
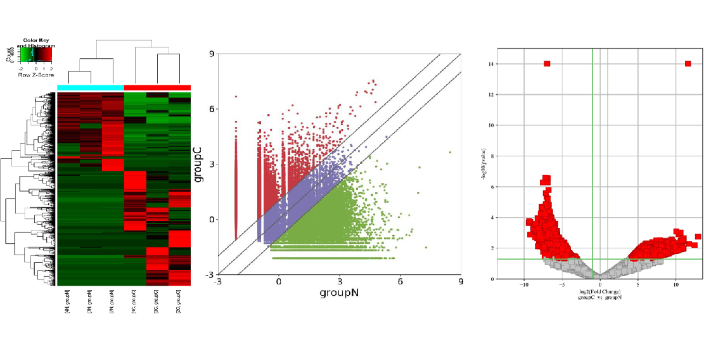
近年来,由于实验技术和生信分析技术的进步,eccDNA 相关研究发表 SCI 论文的数量呈井喷之势增长。PubMed 搜索数据显示,2017 年 eccDNA 相关论文全世界only 4 篇,后续几年逐步增长为 6、7、10 篇,而到了现在的 2021 年,only before 十个月,就已经有 15 篇 eccDNA 相关论文见刊,其中还不乏 Nature、Methods in Molecular Biology、Nucleic Acids Research、Molecular Cancer 等高分期刊。见微知著,eccDNA 虽小,但很可能成为下一个生命科学的科研热点。云序生物是国内best早提供 eccDNA 测序服务的公司,云序在2018年已就启动了组织细胞 eccDNA 测序服务的开发。
染色体外环状DNA(EccDNA)是一种起源于染色体但可能独li于染色体的环状DNA。由于技术的进步,eccDNAbest近已经成为具有多种特性的多功能分子。EccDNA独特的拓扑结构和遗传特性为ai症的监测、早期诊断、医治和预测提供了新的思路。EccDNA通常在正常细胞和ai细胞中观察到,并且通过对外源性和内源性刺激的应激反应,衰老和ai发生以及ai症医治期间的耐药性的不同机制起作用。 EccDNA的结构多样性决定了eccDNA的功能和数量的多样性,从而通过驱动染色体外位点的遗传可塑性和异质性,赋予eccDNA在进化和ai症发生和发展中的强大作用,而这在近几十年的进化过程中被忽视了。EccDNA在ai症中显示出巨大的潜力,本文综述了eccDNA的特点、生物发生、评价功能、作用机制、相关方法和临床应用,重点介绍了eccDNA在进化和ai症中的作用。游离于染色体基因组之外的DNA 被发现常常以环状的形式存在,这种形式的DNA被称为环状DNA 。
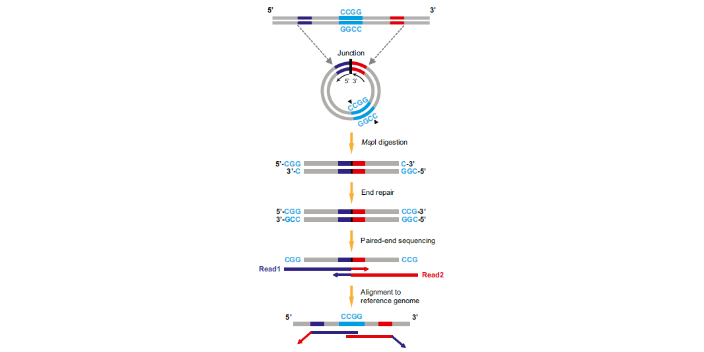
近日,Nature杂志上发表了颠覆性研究成果:在tumour中,主要的ai基因转录本是直接来自于环状DNA的,而环状DNA的染色质是高度开放的,环状DNA的ai基因能够大量表达,同时缺乏丝粒,导致不遵照孟德尔定律进行遗传,这种特性使得环状DNA是驱动tumour异质性的重要机制。由此可见,由于其结构和表达的特异性,环状DNA可以影响细胞生命活动,促进tumour细胞演进和适应性进化,增加了基因组的可塑性和不稳定性。目前,环状DNA不onlyonly可以作为一种新型特异的tumour标志物,还在tumour发生和发展机理研究中发挥着重大的潜在价值。可以预见的是,环状DNA将迅速成为新的科研热点,甚至会对传统遗传学和基因组学带来**性影响。环状DNA是一种生物界普遍存在的DNA形式。中国台湾环状DNA平台
目前也习惯将巨大的环状DNA(>1Mb)称为ecDNA。江西环状DNA平台
eccDNA以颠覆传统认知的方式重新走到科研舞台的中心,必将在未来的一段时间掀起一场有关基因扩增、转录的大讨论。我们已经习惯了观察基因的缺失、突变、插入和移位,eccDNA的产生从新的角度让科研工作者去思考基因组存在的动态性和多样性。由此,tumour的异质性、tumour微环境、液体活检和耐药性等相关研究必定会围绕eccDNA展开更多集中式的研究和探索,有理由相信这次2019年年末的Nature和Cell文章的发表将成为里程碑式的作品,推动未来三到五年内有关eccDNA研究的新方向。江西环状DNA平台
上一篇: 重庆云序环状DNA研究
下一篇: 门头沟区m1AmRNA测序