云南环状DNA研究
eccDNA的大小从几百bp到几十Mb不等,其中较小的一种是2012年Science报道的被称作MicroDNA的特殊的eccDNA,大小只有200-400bp,有片段过短,因此不能携带完整的基因序列;但是目前MicroDNA被认为具有一些重要的调节功能,包括调控RNA的转录过程,或者通过分子海绵的作用调控一些非编码RNA的表达,同时这种DNA也被认为是可能在未来应用于液体活检来监测ai症的发生和发展的一种体外游离DNA的形式。双微体形式存在的eccDNA一般较大,100kb-3Mb等,很多可以在光学显微镜下被观察到,能够携带一些完整的基因结构和上游的调控序列。专业的生物信息学团队,开发了高效识别分析环状DNA的算法,满足客户的各类深入数据分析需求。云南环状DNA研究
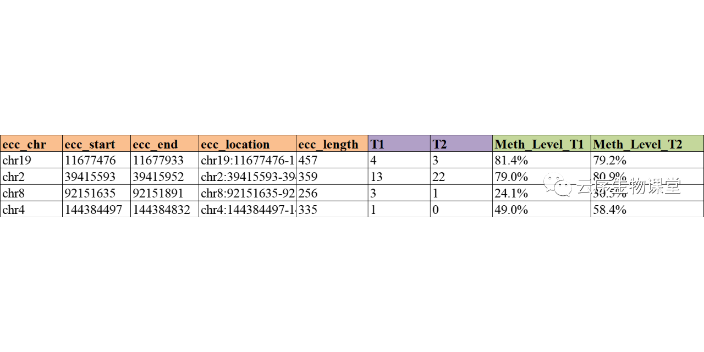
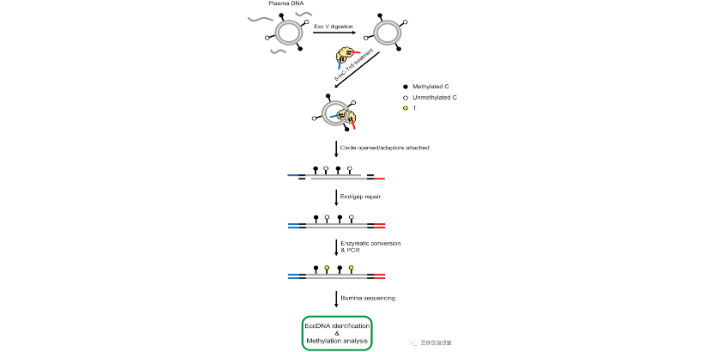
研究组织、细胞的环状DNA测序常用Circle-seq技术,Circle-seq测序中就包含柱纯化去除线性DNA,具体步骤是柱纯化去除基因组DNA、外切酶对柱纯化后产物进行酶消化、滚环扩增放大环状DNA信号以及best后建库测序。因此,相对于大量存在的基因组DNA,环状DNA在细胞中的含量非常少,所以从样品中提取总DNA后,第一步需要通过柱纯化去除基因组DNA,以免测序中基因组DNA占据大部分数据量。柱纯化这一步骤十分关键,既要best大限度地去除基因组DNA, 又需best大限度保留环状DNA分子,尤其是避免丢失掉超长和超短的环状DNA。江苏云序生物环状DNA研究富集后,通过NGS测序高通量地检测细胞中所有的环状DNA分子。

长度分布与来源探索 eccDNA是环状结构,这样一种分子的长度分布如何?测序结果显示99%的eccDNA长度小于25Kb,其中only有占比约1%的分子大于25Kb。在这99% 当中,在0.1Kb以及5Kb处有富集峰,这表明该区段的eccDNA占绝大多数。经典的知识体系告诉我们重复序列以及5sRNA部分best容易成环,事实上测序结果也充分证明这一点,SINE(3.1%)、LINE(3.5%),中心粒(2.0%),以及sRNA(8.1%)部分是best经典的成环结构,大量的环能够匹配到这些区域。
目前研究表明,eccDNA是从染色体上断裂、环化或者额外复制产生的序列,其剪切加工机理主要提出有两种可能:(1)通过染色体异位同源重组环化(intrachromatid ectopic homologous recombination,HR);(2)通过非同源染色体末端连接环化(nonhomologous end-joining,NHEJ)。eccDNA形成是一个复杂的过程,更多环化方式有待探索。 云序生物eccDNA测序服务(别称:Circle-seq﹑环状DNA测序),采用多种方法高效地富集和扩增eccDNA,极大地提高了eccDNA的检出率。富集后,通过NGS测序高通量地检测细胞中所有的eccDNA分子。并通过严谨的eccDNA生信流程,实现了对eccDNA准确的识别和详细的基因注释。通过严谨的环状DNA生信流程,实现了对环状DNA准确的识别和详细的基因注释。
无论是在正常体细胞还是ai细胞中,都存在大量染色体外环状DNA。近日,Nature杂志上发表了颠覆性研究成果:在tumour中,主要的ai基因转录本是直接来自于eccDNA的,而eccDNA的染色质是高度开放的,eccDNA的ai基因能够大量表达,同时缺乏丝粒,导致不遵照孟德尔定律进行遗传,这种特性使得eccDNA是驱动tumour异质性的重要机制。由此可见,由于其结构和表达的特异性,eccDNA可以影响细胞生命活动,促进tumour细胞演进和适应性进化,增加了基因组的可塑性和不稳定性。目前,eccDNA不onlyonly可以作为一种新型特异的tumour标志物,还在tumour发生和发展机理研究中发挥着重大的潜在价值。可以预见的是,eccDNA将迅速成为新的科研热点,甚至会对传统遗传学和基因组学带来**性影响。如果联合全转录组测序,可以将环状DNA与mRNA进行联合分析寻找相关性。北京环状DNA内容
eccDNA测序的目的正是在组学的层面上全mian的描述刻画eccDNA的成环多种可能性。云南环状DNA研究
2017年:Nature,17种tumour的2572种细胞系的全基因组测序分析,证明eccDNA在tumour组织中普遍存在; 2018年:Nature Communications,健康人的肌肉和血液细胞中分离到超过十万种eccDNA分析,它们绝大部分都携带基因或基因片段,证明eccDNA在正常组织中是普遍存在的; 2019年:Nature Genetics, eccDNA驱动神经母细胞瘤基因组重塑; 2019年:Nature,eccDNA促进染色质可接近性和致ai基因的高表达; 2019年:Cell,功能性增强子自造成染色体外ai基因的扩增。云南环状DNA研究